Un bleu cyan d’origine naturelle pour remplacer un colorant synthétique
Le bleu cyan est une des couleurs primaires avec le magenta et le jaune que l’imprimerie comme l’imagerie informatique utilisent pour la synthèse des couleurs. Cette couleur, qu’on rencontre relativement peu dans la nature, est obtenue dans l’industrie alimentaire grâce à un colorant de synthèse, le bleu brillant FCF ,dont la longueur d’onde d’absorption maxima λmax vaut 630 nm. Il est utilisé en particulier dans la pâtisserie pour obtenir des colorations bleues ou vertes. Tous les colorants naturels bleus connus ont une longueur d’onde d’absorption maxima λmax inférieure à 630 nm. Des chercheurs de l’University of California, Davis, USA associés à une équipe internationale ont proposé d’utiliser une anthocyanine présente dans le chou rouge.
Les anthocyanines du chou rouge
Dans le chou rouge, on trouve des molécules organiques nommées anthocyanines qui ont toutes une couleur pourpre ou violette. Un long travail d’analyse spectrométrique et chromatographique a permis aux chercheurs de déterminer 8 types d’anthocyanine dans le chou rouge et leurs qualités colorantes respectives. Ces 8 anthocyanines, notées de P1 à P8 correspondent à la présence dans la molécule de la figure 1 de différentes paires de radicaux R1 et R2.
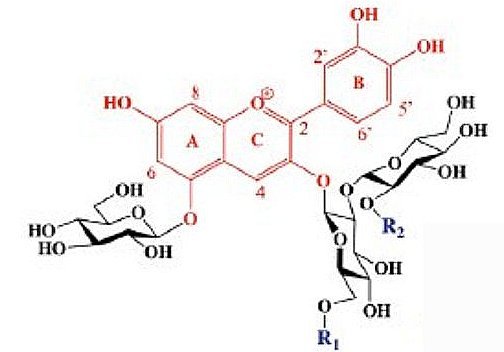
Fig.1. Structures des anthocyanines du chou rouge
R1 et R2 sont des radicaux correspondant aux 8 anthocyanines P1 à P8. Dans le cas de l’anthocyanine P2, R1 est l’ion hydrogène H et R2 est le radical sinapoyl
Tiré de Discovery of a natural cyan blue: A unique food-sourced anthocyanin could replace synthetic brilliant blue Pamela R. Denish, Justin B. Siegel et al.
Sci. Adv. 2021; 7 : eabe7871 7 April 2021 Creative Commons Attribution License 4.0 (CC BY).
Les anthocyanines sont des colorants dont les teintes sont variables en raison de l’équilibre entre leurs différentes formes. Ces chromophores naturels sont généralement colorés dans le rouge dans des conditions acides et tirent vers le violet et le bleu quand le pH augmente Dans le chou rouge, leur combinaison produit un bleu intense en solution à pH neutre, mais avec une relativement forte contribution violette qui empêche de l’utiliser en remplacement du bleu FCF.
L’absorption de la lumière par des colorants bleus
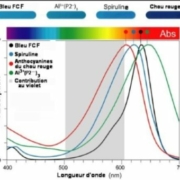
D’ailleurs, les quelques colorants bleus d’origine naturelle ont une forte contribution violette ou des λmax inférieurs à 630 nm, comme on peut le voir sur la figure 2 où l’on a représenté les courbes d’absorption du bleu brillant FCF, de la phycocyanine extraite de l’algue bleue spiruline, de l’ensemble des anthocyanines du chou rouge, et enfin d’une structure tertiaire formée par la liaison entre un ion aluminium Al3+ et 3 anthocyanines du chou P2. Notons qu’un pigment bleu, par exemple, absorbe au maximum dans le rouge magenta qui est sa couleur complémentaire.
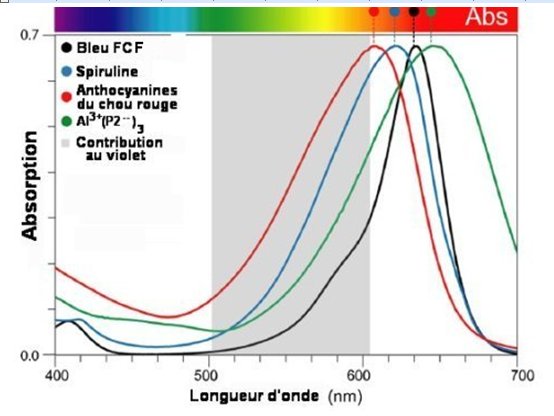
Fig.2. Expression des couleurs pour 4 pigments bleus
Le spectre d’absorption indique les positions en longueur d’onde λmax des maxima d’absorption. Ainsi on a pour le bleu FCF λmax= 630nm, pour la spiruline λmax= 617 nm, pour le chou rouge toutes anthocyanines combinées, λmax= 608 nm à pH 8, enfin pour le complexe Al3+(P2–)3 à pH7 λmax=640 nm.
Tiré de Discovery of a natural cyan blue: A unique food-sourced anthocyanin could replace synthetic brilliant blue Pamela R. Denish, Justin B. Siegel et al.
Sci. Adv. 2021; 7 : eabe7871 7 April 2021 2021 Creative Commons Attribution License 4.0 (CC BY).
Le complexe Al3+(P2—)3
Bien qu’elle figure en proportion mineure dans l’ensemble des anthocyanines du chou rouge, l’anthocyanine P2 ( λmax de 640 nm à un pH de 7) est le composé qui a retenu toute l’attention des chercheurs. P2 a une résistance exceptionnelle à l’addition d’eau, supérieure à celle des autres anthocyanines du chou rouge.
Il était déjà connu que les colorants basés sur les anthocyanines devaient, pour produire une couleur bleue, être de pH neutre et former un complexe avec un ion métallique, tel qu’un Al3+. Le complexe de P2 avec Al3+ s’est avéré bien supérieur à d’autres anthocyanines du chou rouge. La Fig.3 ci-dessous représente la structure chimique de ce complexe.
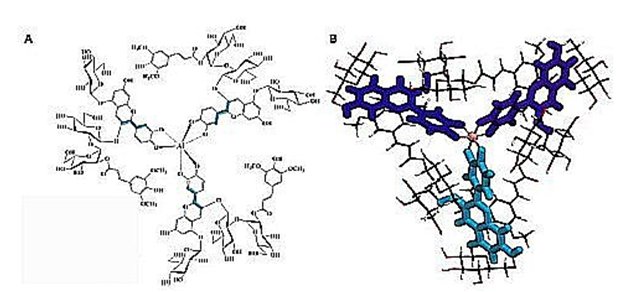
Fig.3. Structure d’ Al3+(P2–)3
A) Structure trimère où 3 molécules P2 forment une structure en forme d’hélice autour de l’ion aluminium.
B) Représentation 3D des anthocyanines P2 autour de l’aluminium.
Tiré de Discovery of a natural cyan blue: A unique food-sourced anthocyanin could replace synthetic brilliant blue Pamela R. Denish, Justin B. Siegel et al.
Sci. Adv. 2021; 7 : eabe7871 7 April 2021 2021 Creative Commons Attribution License 4.0 (CC BY).
La longueur d’onde d’absorption maxima de Al3+(P2—) est supérieure de plus de 20 nm à celle des complexes d’Al3+ avec les anthocyanines P5 et P8, par ailleurs les mieux placées.
La stabilité dans le temps de Al3+(P2—)3 est plus forte aussi.
L’un des problèmes rencontrés était celui de la faible proportion (5%) de P2 dans le contenu total d’anthocyanines du chou rouge. La solution très élégante apportée par les chercheurs à ce problème a été une méthode enzymatique d’enrichissement par conversion des anthocyanines P6, P7 et P8 en P2.
Le nouveau colorant a une remarquable stabilité. Après de plus de 55 jours dans du sirop de sucre à pH 7, il ne perd que 14% de sa couleur. On a pu l’utiliser pour obtenir des couleurs bleues et vertes dans plusieurs aliments sans observer de décoloration après 30 jours à température ambiante. Le stockage en milieu acide augmente encore la stabilité du colorant et il est toujours possible de le ramener au pH neutre avant l’intégration dans le produit à colorer.
Cette méthode permet de produire à partir d’une source naturelle un nouveau colorant bleu cyan dont les propriétés sont quasi identiques à celle du colorant synthétique bleu brillant FCF. Ce colorant permet aussi d’obtenir des couleurs vertes de qualité.
Pour en savoir plus :
Discovery of a natural cyan blue: A unique food-sourced
anthocyanin could replace synthetic brilliant blue
Pamela R. Denish1, Julie-Anne Fenger, Randall Powers, Gregory T. Sigurdson,
Luca Grisanti, Kathryn G. Guggenheim, Sara Laporte, Julia Li, Tadao Kondo,
Alessandra Magistrato, Mícheál P. Moloney, Mary Riley, Mariami Rusishvili6,
Neda Ahmadiani5, Stefano Baroni, Olivier Dangles, Monica Giusti, Thomas M. Collins,
John Didzbalis, Kumi Yoshida, Justin B. Siegel, Rebecca J. Robbins,
Science Advances 2021; 7 : eabe7871 7 April 2021